問題 1.
次の文を完成させなさい。
ベンゼンの化
混酸(濃+濃硝酸)にベンゼンを加え、よく振る。
⇓
約℃の湯浴で温める。
⇓
ベンゼンが生成する。
⇓
冷水に注ぐとベンゼンが沈む。
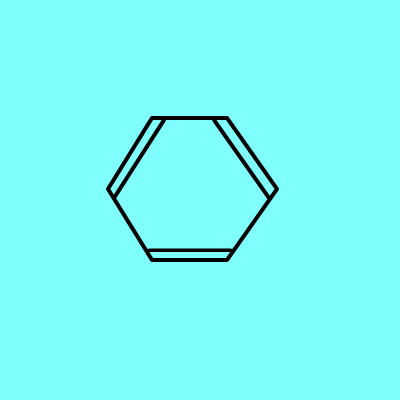 |
|
+ HNO3 ⇒ |
|
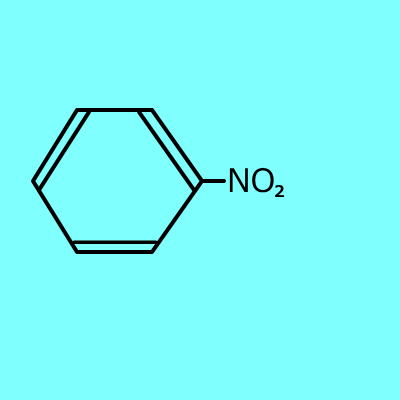 |
|
+ H2O |
|
| ベンゼン |
|
|
|
ベンゼン(沸点211℃) |
特有のにおいをもつ性の色の液体。水に難溶であるが、有機溶媒には溶けやすい。
問題 2.
ベンゼンの化
 |
|
+ H2SO4 ⇒ |
|
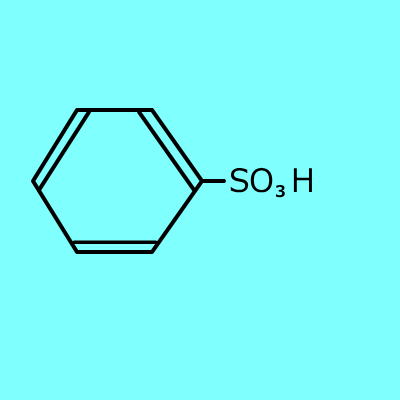 |
|
+ H2O |
|
| ベンゼン |
|
|
|
ベンゼン酸 |
| |
|
|
|
|
|
|
|
| |
|
|
|
(-SO3H:基) |
濃にベンゼンを加える。
⇓
振り混ぜながら、する。
⇓
ベンゼン酸が生成する。
⇓
ナトリウム水溶液に生成物を少しずつ注ぐ。
⇓
すると、ナトリウム塩が析出し、状になる。
 |
|
+ NaCl ⇒ |
|
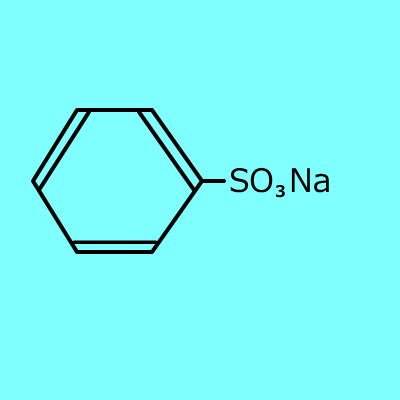 |
|
+ HCl |
|
| ベンゼン酸 |
|
ベンゼン酸 |
| |
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
ベンゼン酸は水への溶解度が非常に、そのままでは析出させることができない。そのため、塩化ナトリウム水溶液の中に注ぎ入れ、ナトリウムの形でさせる。
問題 3.
ベンゼンの化
臭素との置換反応
臭素を発生させた水溶液にベンゼンを加える。
⇓
水溶液を加え、よくかき混ぜて反応させると、ベンゼンが生成する。
⇓
生成したベンゼンをジエチルエーテルでする。
⇓
ジエチルエーテルをさせ、を加えるとベンゼンがビーカーの底に得られる。
 |
|
Br2 + AgNO3 |
⇒ |
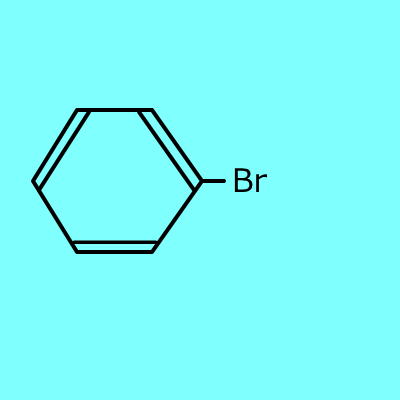 |
|
+ AgBr + HNO3 |
|
|
| ベンゼン |
|
|
|
ベンゼン |
|
臭化銀 硝酸 |
|
|
| |
|
|
|
(密度:1.50g/cm3) |
|
|
|
|
塩素との置換反応
| |
|
|
触媒 |
|
|
|
|
 |
|
+ Cl2 |
⇒ |
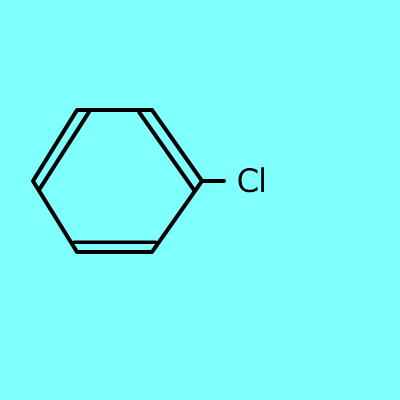 |
|
+ HCl |
|
| |
|
|
|
ベンゼン(沸点:132℃) |
ベンゼンにを作用させると、水に難溶の無色の液体であるベンゼンが生じる。
ベンゼン
ベンゼンに塩素を作用させるとp-ジクロロベンゼンが得られる。性があり、衣類の剤として用いられる。
 |
|
+ Cl2 ⇒ |
|
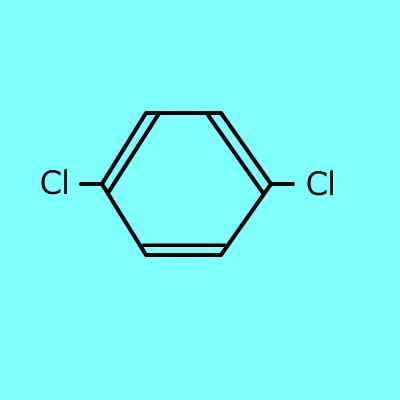 |
|
+ HCl |
|
| |
|
|
|
p-ジクロロベンゼン(融点:54℃) |
お疲れ様でした。「採点」ボタンを押して採点してください。
